Кровь на бактериальный посев при сепсисе необходимо забирать
Обновлено: 05.10.2024
Постановка (или предположение) диагноза сепсиса входит в функциональные обязанности врача любой специальности вне зависимости от стажа и места работы. Следует подчеркнуть, что указанные в предыдущем разделе клинико-лабораторные критерии не являются высокоспецифичными для сепсиса. Тем не менее, регистрация этих критериев служит основанием для предположения диагноза сепсис и начала диагностического поиска инфекционного очага.В настоящее время международным экспертным сообществом настоятельно рекомендуется ежедневный скрининг тяжелых пациентов, имеющих риск инфицирования, особенно пациентов, госпитализирован-ных в ОРИТ, для своевременного выявления как минимум клинических признаков сепсиса и как можно более раннего начала адекватной антимикробной и патогенетической терапии.Минимальный объем исследований, который должен быть выполнен при подозрении на сепсис включает в себя:
− общий анализ крови с тромбоцитами (имеет место снижение уровня тромбоцитов);
− коагулограмму (отмечается удлинение АЧТВ, протромбинового и тромбинового времени, снижение содержания фибриногена и повышение уровня D-димеров);
− определение группы крови и Rh-фактора;
− биохимический анализ крови (общий белок, альбумин, общий и прямой билирубины, мочевина, креатинин, натрий, калий, кальций, хлор, трансаминазы, глюкоза);
− КОС (рН и газы артериальной крови);
− рентгенографию органов грудной клетки;
− микроскопию и посев материала из предполагаемого первичного очага;
Микробиологическое исследование крови.
Клиническая значимость регистрации бактериемии:
− подтверждение диагноза и определение этиологии инфекционного процесса;
− доказательство механизма развития н(апример, катетер-ассоциированый сепсис);
− для некоторых ситуаций аргументация тяжести течения патологического процесса (например, инфекционный эндокардит);
− обоснование выбора или смены режима антибиотикотерапии;
− оценка эффективности терапии.
Отсутствие бактериемии не должно исключать возможность диагноза при наличии критериев сепсиса! При соблюдении строгих требований к правильному забору мате-риала и использовании современных микробиологических методик положительнаягемокультура при сепсисе наблюдается более чем в 50 % случаев. При выделении типичных патогенов (Staphylococcusaureus,Streptococcuspneumoniae, Klebsiellapneumoniae, Pseudomonasaeruginosa,Acinetobacterbaumannii, грибы) для постановки диагноза, как правило, достаточно одного положительного результата. Однако при выделении микроорганизмов, являющихся кожными сапрофитами и способных кон-таминировать образец (Staphylococcusepidermidis, другие коагулазонегативные стафилококки, дифтероиды), для подтверждения истинной бактериемии требуются как минимум две положительные гемокультуры.
Показания для забора крови на стерильность:
− признаки полиорганной дисфункции.
Для проведения адекватного микробиологического исследования крови следует строго соблюдать следующие правила:
1. Кровь для исследования необходимо брать до назначения антибиотиков. Если больной уже получает антибактериальную терапию, то кровь следует брать непосредственно перед очередным введением препарата.
2. Стандартом исследования крови на стерильность является забор материала из двух периферических вен с интервалом до 30 мин, при этом из каждой вены кровь необходимо отбирать в два флакона (со средами для выделения аэробов и анаэробов).
Забор крови на самом пике лихорадки не повышает чувствительности метода.
3. Дополнительно рекомендуется произвести забор крови из каждого сосудистого катетера, если он был установлен за 48 ч или более до исследования.
4. Кровь для исследования необходимо брать из периферической вены. Не показано преимуществ забора крови из артерии.
5. Брать кровь из периферической вены следует, тщательно соблюдая правила асептики. Кожу в месте венепункции дважды обрабатывают раствором йода или повидон-йода концентрическими движениями от центра к периферии в течение 1 мин. Непосредственно перед забором кожу обрабатывают 70%-ным спиртом. Каждую пробу (около 10 мл крови или в объеме, рекомендованном инструкцией производителя флаконов) забирают в отдельный шприц.
6. При наличии установленного (предполагаемого) инфекционного очага следует проводить микробиологическое исследование субстрата (мочи, ликвора, мокроты и т. д.) из вероятного очага инфекции и периферической крови. Если из предполагаемого очага инфекции и периферической крови выделяется один и тот же микроорганизм, его этиологическую роль в развитии сепсиса следует считать доказанной.
7. При наличии факторов риска грибковой этиологии сепсиса дополнительно следует выполнять посев крови на специальные селективные среды (среда Сабуро). Биологические лабораторные маркеры сепсиса. Одним из наиболее значимых ограничений использования бактериологического исследования крови для подтверждения диагноза является продолжительное время, необходимое для выполнения данного исследования (не менее 72 ч). Кроме того,гемокультура может быть ложноотрицательной у пациентов, заболевание которых вызвано медленнорастущими микроорганизмами, микроорганизмами, требующими особых условий культивирования или присутствующими в малых концентрациях, а также у пациентов, получающих на момент взятия крови для исследования антимикробную терапию. Вследствие этого в настоящее время наблюдается интенсивное развитие методик, основанных на определении различных биологических лабораторных маркеров (биомаркеров). Существующие биомаркеры сепсиса позволяют более эффективно исключать наличие инфекции, чем подтверждать ее присутствие, т. е. обладают в основном отрицательной предикативной ценностью. Помимо этого, биомаркеры потенциально могут использоваться для прогнозирования развития органной дисфункции, определения режима эмпирической антибактериальной терапии, а также для контроля за эффективностью проводимого лечения.
В табл. 1суммированыбиомаркеры сепсиса, эффективность которых продемонстрирована как минимум в одном клиническом исследовании.
Однако из перечисленных в табл.1 биомаркеров сепсиса только некоторые имеют доказательную базу, основанную на крупных международных рандомизированных исследованиях, и широко внедрены в клиническую практику:С-реактивный белок ипрокальцитонин (ПКТ) — преимущественно для идентификации бактериальной этиологии, маннан/антиманнан и 1,3-β-D-глюкан — для грибковой этиологии сепсиса. Однако стоит отметить, что даже эти маркеры не являются строго специфичными для подтверждения наличия инфекции и, соответственно, сепсиса.
Концентрация С-реактивного белка в сыворотке крови свыше 87 мг/л указывает на наличие инфекции с чувствительностью 93,4 % и специфичностью 86,1 %, а ее комбинация с лихорадкой более 38,2 °С повышает специфичность методики до 100 %. Учитывая неспецифичность С-реактивного белка, изменения его уровня в динамике обладают большей диагностической ценностью, чем однократное определение. Увеличение уровня свыше 41 мг/л указывает на развитие инфекции с чувствительностью 92,1 % и специфичностью 71,4 %, а повышение при повторном измерении свыше 87 мг/л — с чувствительностью и специфичностью 92,1 и 82,1 % соответственно.
В ряде исследований было также убедительно продемонстрировано, что повышение уровня С-реактивного белка свыше 100 мг/л с высокой степенью вероятности свидетельствует о бактериальной этиологии сепсиса, до 100 мг/л — о грибковой этиологии. Однако уровень С-реактивного белка как острофазового повышается практически при любом состоянии, сопровождающемся развитием воспалительной реакции, в том числе при ревматоидном артрите. Кроме того, его повышение происходит через 12–24 ч от начала инфекционного процесса, что резко снижает его диагностическую ценность в начальном периоде сепсиса, когда эффект от начатой антимикробной терапии максимален.
ПКТ представляет собой предшественник гормона кальцитонина и присутствует в сыворотке крови здоровых людей в очень низких концентрациях (0,033 нг/мл). Однако при развитии инфекционного процесса в течение 2–4 ч его уровень повышается более чем в 1000 раз, достигая пика через 6–8 ч. Пороговым значением, указывающим на необходимость назначения антибактериальной терапии при наличии клинической симптоматики, служит повышение уровня ПКТ свыше 0,25 мкг/л. При значении ПКТ ниже 0,25 мкг/л, но сохраняющемся подозрении на наличие бактериальной инфекции, рекомендуется повторно определить уровень ПКТ через 6–24 ч. При отсутствии повышения уровня в динамике вероятность наличия бактериальной инфекции не превышает 5 %.
Рекомендуется динамическое определение уровня ПКТ (1 раз в2–3 дня) у пациентов, находящихся на антибактериальной терапии, для контроля за эффективностью проводимого лечения и определения времени отмены антибиотика. Снижение ПКТ на 25–35 % в течение 3 дней указывает на эффективность проводимой антибактериальной терапии. Снижение ПКТ на 80–90 % от максимального уровня, зафиксированного у данного пациента, может служить основанием для отмены антибактериальных препаратов.
Определение ПКТ особенно актуально для дифференциальной диагностики бактериального сепсиса, однако необходимо учитывать, что его уровень может быть ниже порогового значения (0,25 мкг/л) у пациентов с дыхательной или сердечно-сосудистой недостаточностью, а также у пациентов с тяжелыми множественными сопутствующими заболеваниями, что связано с более медленным ростом уровня ПКТ у данной категории пациентов.Кроме того, ложноотрицательные низкие уровни ПКТ могу наблюдаться на ранних этапах инфекционного процесса (в первые 6 ч), у пациентов с подострым эндокардитом, а также при локализованных инфекциях. Высокие ложноположительные уровни ПКТ могут наблюдаться у пациентов:
− в первые 72 ч после серьезной травмы, обширного хирургического вмешательства, тяжелых ожогов, применения иммуноглобулинов и прочих лекарственных средств, стимулирующий выделение провоспалительных цитокинов;
− с инвазивными грибковыми инфекциями;
− с малярией, вызванной Pl. falciparum;
− с продолжительным или тяжелым кардиогенным шоком, продолжительным нарушением кровоснабжения органов;
− с мелкоклеточным раком легкого или с C-клеточной карциномой щитовидной железы;
− с острым панкреатитом;
− с инфарктом миокарда;
− рецепиентов после пересадки почки;
− новорожденных детей в первые 48 ч после рождения.
В вышеперечисленных случаях установления как ложноотрицательных, так и ложноположительных значений ПКТ при наличии подозрения на бактериальный сепсис также рекомендуется повторить определение уровня ПКТ через 6–24 ч. При отсутствии динамики уровня ПКТ назначение/продолжение антибактериальной терапии не показано.
Ввиду того, что для выполнения микологического исследования крови необходимо время (не менее 5 суток), а его чувствительность не превышает 50–75 %, при подозрении на грибковую этиологию сепсиса и наличии возможности одновременно с посевом крови на специальную питательную среду необходимо выполнить определение уровня 1,3-β-D-глюкана илиманнана/антиманнана в сыворотке крови ввиду высокой отрицательной предикативной ценности обоих методов в отношении наиболее частых возбудителей грибковых инфекций в общесоматических стационарах Candidaspp. и Aspergillusspp. Определение маннана/антиманнана позволяет определить наличие инвазивной грибковой инфекции в среднем за 6–9 дней до появления положительной гемокультуры (чувствительность и специфичность данного метода составляют 73–80 и 80–85 % соответственно). Определение 1,3-β-D-глюкана также позволяет выявить с относительно высокими чувствительностью (> 62,5 %) и специ-фичностью (> 80 %) наличие инвазивной грибковой инфекции на 1–3 дня раньше по сравнению с методом гемокультуры.
В случае отрицательного результата определения маннана/антиманнана у пациента с факторами риска грибковой инфекции и наличием поражения легочной ткани (особенно в виде первичного септического очага) целесообразно дополнительно определить уровень галактоманнанав сыворотке крови.
Однако при этом следует помнить, что вышеуказанные методы не позволяют подтвердить или исключить грибковые инфекции, вызванные рядом сравнительно более редких возбудителей (игомицеты, Cryptococcusspp. и др.), чаще встречающихся в специализированных стационарах (гематологических, онкологических, инфекционных и т. д.). Кроме того, основным отрицательным моментом определения маннана и антител к нему является высокая частота (более 20 %) ложноположительных и ложноотрицательных реакций.
Ложноположительные результаты исследования на 1,3-β-D-глюканимеют место:
− после инфузии пациенту раствора альбумина, иммуноглобулинов;
− при использовании марлевых повязок;
− при нахождении пациента на гемодиализе.
Кроме вышеперечисленныхбиомаркеровдостаточно широко обсуждается возможность использования в диагностике сепсиса пресепсина. Данный маркер является чрезвычайно перспективным с позиций патофизиологии сепсиса, так как представляет собой продукт превращений мембранного белка (рецептора) моноцитов/макрофагов (mCD14) под воздействием эндотоксинов бактериальной клетки, уровень которого повышается только при воспалительных процессах, сопровож-дающихся фагоцитозом, и коррелирует с их выраженностью и тяжестью течения. Однако данные проведенных в отношении пресепсина клинических (в большинстве случаев небольших по объему) и лабораторных исследований несколько противоречивы, что требует более углубленного изучения данного биомаркера и не позволяет однозначно рекомендовать его для использования в клинической практике.
Другие методы диагностики сепсиса. В диагностике сепсиса также возможно использовать методики, основанные на исследовании крови с помощью полимеразной цепной реакции в реальном времени (SeptiFast®, SeptiTest® и др.) или гибридизации insitu (например, PNA-FISH — Peptidenucleicacidfluorescentinsituhybridization), которыепозволяютопределитьэтиологию септического процесса в течение нескольких часов после забора материала от пациента, причем их чувствительность и специфичность достигает 94–99 и 98 % соответственно.
Однако в настоящее время данные методики можно применять лишь как дополнение к традиционному микробиологическому исследованию, так как они отлично идентифицируют микроорганизм, но неспособны дать детальную информацию о его чувствительности к антимикробным препаратам, ограничиваясь определением лишь нескольких наиболее ключевых маркеров резистентности (например,генов отвечающих за продукцию металло-β-лактамаз или сериновыхкарбапенемаз у грамотицательных бак-терий, гена, отвечающего за модицификацию пенициллин-связывающего белка уметициллин-резистентных стафилококков и т. д.). Дополнительными негативными моментами являются: способность идентифицировать только заранее предопределенный спектр микроорганизмов и относительно высокая вероятность ложноположительных результатов исследования в связи с контаминацией.
Врач лаборант ЦДЛ городской больницы
Константин Костюк
Приемная главного врача
(+375 214) 50-62-70
(+375 214) 50-62-11 (факс)

17 сентября 2019 г. в журнале Annals of Internal Medicine опубликована статья "Результаты посевов крови до и после введения противомикробных препаратов у пациентов с тяжелыми проявлениями сепсиса".
Среди врачей идут постоянные споры, где врачи, оказывающие изначальную помощь пациентам с сепсисом, стремятся ввести противомикробные препараты как можно быстрее с целью профилактики смертности, в то время как врачи ведущие данных больных позже, предпочитают забор крови на посев до введения антибиотиков, чтобы более точно определить ответственный микроорганизм.
Введение противомикробных препаратов до забора крови на посев может потенциально снизить время до начала лечения и улучшить исходы, но непонятно как данная стратегия повлияет на диагностическую чувствительность.
В представленном исследовании, которое прошло в 7-ми стационарах США и Канады, решили сравнить как изменится диагностическая точность посева крови у пациентов с сепсисом, если сначала ввести антибиотик и затем быстро взять кровь на посев, и сравнить с изначальным забором крови на посев и только потом вводить антибиотики.
В исследовании участвовали 325 пациентов (средний возраст 65,6 лет) с тяжелыми проявлениями сепсиса, включая систолическое АД менее 90 мм рт ст или уровень лактата сыворотки 4 ммоль/Л или более. Всем пациентам делали забор крови на посев дважды до начала введения антибиотиков, и затем дважды в течение -2х часов после начала эмпирической антибиотикотерапии.
- при заборах крови до введения антибиотиков, посев был положителен на 1 или более микробов у 31,4 % пациентов.
- при заборах крови после введения антибиотиков посев был положителен на 1 или более микробов у 19,4 % пациентов.
Авторы заключают, что у пациентов с тяжелыми проявлениями сепсиса, эмпирическая противомикробная терапия значительно снижает чувствительность посевов крови, если кровь была взята вскоре после начала антимикробной терапии.
Исходя из данных результатов можно сделать вывод, что нужен баланс между отрицательными последствиями от затягивания противомикробной терапии ввиду ожидания забора крови на посев, и получением отрицательного результата посевов, если противомикробная терапия была начата без ожидания забора крови на посев. Очень важным является быстрый забор крови хотя бы на один посев до начала противомикробной терапии.
Инфекционное заражение крови, или, более точно, сепсис – состояние, реально угрожающее жизни человека. В онкологии сепсис – результат проникновения в организм человека патогенных микроорганизмов. Именно они провоцируют началу выработки биологически активных веществ, так называемых медиаторов воспаления.
Наши ткани и органы очень активно реагируют на данный процесс, из-за чего в разных частях тела появляются воспалительные очаги. Они-то и вызывают дисбаланс жизненно важных функций. Как уже отметили, в такой ситуации очень возможен летальный исход.
Врачу-онкологу важно уделять особое внимание диагностическим процедурам и лечению сепсиса, ведь именно он довольно часто возникает у онкобольных. Группу риска составляют прооперированные пациенты, находящиеся в терапевтической палате. Даже теоретически невозможно создать стерильные условия идеальные. И здесь задача врачей – применить новейшую диагностику заболевания и умение принять нужные меры по решению данной проблемы.
Почему возникает
Возникновение сепсиса вызывают микроорганизмы. Это и паразиты, и грибы, и бактерии, и вирусы, в большинстве случаев приникающие в организм из внешней среды.
Иногда сепсис развивается от естественной флоры организма, происходит это обычно при чрезвычайно сниженном иммунитете.
Не стоит думать, что сам факт проникновения инфекции в наш организм инициирует сепсис. Существуют дополнительные факторы, приводящие к генерализации данного процесса.
Здесь мы говорим, прежде всего, о группе риска:
- Возраст 75+;
- Травмы;
- Ожоги;
- Алкоголизм;
- Наркомания;
- Заболевания хронического характера;
- Проведенные операции;
- Наличие инвазивных устройств;
- Длительное лечение в клинике;
- Сбой системы иммунитета, вследствие заболеваний или проведенной химиотерапии;
- Беременность, роды.
Виды сепсиса
Классификация заболевания строится на локализации первичного очага:
Если при первичном нельзя установить локализацию очага, то при сепсисе вторичном в зависимости от его местоположении классифицируют:
- Чрескожный. Очаг – на коже;
- Одонтогенный. Причина возникновения – болезни зубочелюстной системы;
- Отогенный. Воспаление в ухе;
- Гинекологический сепсис. Очаг – в женских половых органах;
- Хирургический. Инфицирование в ходе хирургической операции или проведения процедур инвазивного характера.
Когда назначают анализ
Бывает, что симптомы сепсиса слабо проявляются и напоминают проявления других заболеваний.
Симптомы, которые должны насторожить врача и назначить анализы:
- Повышение температуры тела;
- Учащающееся дыхание и сокращения сердечной мышцы;
- Обильная потливость;
- Признаки дисфункции различных органов.
В ситуациях тяжелых у пациента наблюдаются:
- Вялость;
- Спутанность сознания;
- Снижение артериальное давление;
- Холод в конечностях, синюшность;
- Появление пятен на коже.
Немаловажная причина назначить анализы на выявление сепсиса – ранее проведенные исследования позволяют заподозрить заражение крови.
Как правило, для исследования применяются критерии шкалы quick SOFA (qSOFA), где важно выявить 3 критерии, суммарно подтверждающих наличие сепсиса:
- Верхнее артериальное давление ниже 100 мм рт. ст.;
- Частота дыхания до 22 в минуту;
- Изменение мышления.
Для более точной постановки диагноза используют критерии шкалы SOFA, в которых учтены результаты лабораторных анализов.
Процедура проведения анализа
Международный метод количественной диагностики бактериальных токсинов – анализ активности эндотоксина (EАА). Это единственный на сегодняшний день метод, одобренный Управлением по контролю качества пищевых продуктов и медикаментов США.
Эндотоксин – липополисахарид по своей химической природе. Он является сильным медиатором воспалительного процесса. И даже на начальных этапах развития сепсиса его уровень резко повышается.
Анализ на уровень эндотоксина представляет собой забор крови с последующим добавлением в нее уникальных антител, которые, связываясь с бактериальным липополисахаридом, поглощают нейтрофилы.
Благодаря этому в клетках начинаются биохимические реакции и происходит быстрое поглощение и расходование кислорода.
Интенсивность возникающего свечения, которое регистрируют посредством люминометра, дает возможность судить об уровне эндотоксина в крови.
Полученный в ходе исследования результат оценивают от 0 до 1:
0– эндотоксин отсутствует;
менее 0,4 – уровень низкий;
0,4–0,59 – уровень промежуточный;
0,6 и более – уровень высокий;
1 – уровень критический.
Проведение данного анализа не вызывает сложностей.
- Быстрое получение результатов;
- Простота;
- Информативность;
- Выявление риска развития сепсиса;
- Диагностика сепсиса на ранних его стадиях.
Клиника Onco.Rehab имеет все необходимое для проведения данного анализа на сепсис.
Эритроциты при сепсисе
Эритроциты – кровяные клетки, содержащие гемоглобин и отвечающие за продвижение кислорода и углекислого газа.
При развитии сепсиса на поздних стадиях они разрушаются. Прежде всего, происходит:
- Анемия, т.е. гемоглобин снижается;
- Уменьшение количества эритроцитов;
- Возникает свободный гемоглобин, который активизирует выработку веществ, с воспалением связанных;
- Снижение их деформирования, а значит, и их основных функций.
СОЭ при сепсисе
СОЭ, или скорость оседания эритроцитов (мужская норма 2–15 мм/час, женская 1–10 мм/час.) при заражении крови повышается. Это явный показатель того, что в организме происходит воспалительный процесс.
Лейкоциты при сепсисе
Увеличение количества лейкоцитов в крови вызывает лейкоцитоз. Причиной увеличения этих белых кровяных телец – развитие процесса воспаления.
В ряде случаев уменьшается особого вида лейкоцитов, нейтрофилов приводит к нейтропении. Это плачевный симптом.
Тромбоциты при сепсисе
Тромбоцитопения, вызванная снижением количества тромбоцитов в крови, – яркий симптом наличия сепсиса.
Риск летального исхода зависит напрямую от того:
Как определить сепсис?
При сепсисе смертность может достигать от 10 до 40%. Зависит это от нескольких важных факторов:
- Вид возбудителя;
- Общее состояние здоровья пациента;
- Время установления диагноза и начала лечения.
Случается, что воспалительный процесс протекает в виде септического шока, при котором наблюдают нарушение кровообращения, обменных процессов в клетках, значительное падение артериального давления. При таком состоянии смертность достигает своего максимального порога.

Посев крови – метод бактериологического исследования, использующийся для достоверного определения наличия бактерий в крови.
Посев используют для выявления в ней различных микроорганизмов приходится делать при многих заболеваниях. Посев крови осуществляют для обособленности, чтобы идентифицировать болезнетворных бактерий при бактериемии.
Бактериемия - это проникновение бактерий в кровь при генерализации инфекции в организме человека, заражении крови (сепсис). Данный вид анализа проводится в лабораториях медицинских учреждений.
Делают посев крови на жидкие питательные среды:
- желчный бульон,
- сахарный бульон,
- жидкие и полужидкие среды для выращивания микробов анаэробов.
Сколько раз нужно сдавать Бак посев крови
Для обнаружения микроорганизмов требуется несколько анализов не менее 3, так как количество бактерий в крови может колеблется.
Определенные виды бактерий можно выделить только специальными бактериологическими посевами (бак посев) крови.
Бак посев крови - что показывает
Бак посев крови показывает чувствительность к антибиотикам той или иной группы бактерий. Определив вид выращенной колоний бактерий после посева, (микробиологического исследования) можно подобрать эффективные антибиотики против именно этой группы микроорганизмов (так называемый посев крови на стерильность).
- Это важно! Перед анализом на посев крови на инфекции - Не принимайте анатибиотики!
Обнаружить бактерии будет трудно или вообще невозможно, если человек перед анализом посева крови принимал антибиотики, при продолжающемся инфицировании болезнетворными микроорганизмами.
Как сдавать кровь на бак посев
Для наиболее точного диагностирования заболеваний недостаточно самого современного лабораторного оборудования.
Точность результатов зависит не только от используемых реактивов и аппаратуры, но и от времени и правильности сбора исследуемого материала. При несоблюдении основных правил подготовки к анализам их результаты могут быть значительно искажены.
Для исследования крови более всего подходят утренние часы
Для большинства исследований кровь берется строго натощак.
Кофе, чай и сок – это тоже еда.
Можно пить воду.
Рекомендуются следующие промежутки времени после последнего приема пищи:
- для общего анализа крови не менее 3-х часов;
- для биохимического анализа крови желательно не есть 12-14 часов (но не менее 8 часов).
За 2 дня до обследования необходимо отказаться от алкоголя, жирной и жареной пищи.
За 1-2 часа до забора крови не курить.
Перед исследованием крови следует максимально снизить физические нагрузки.
- Исключить бег, подъем по лестнице.
- Избегать эмоционального возбуждения.
- Минут10-15 нужно отдохнуть, расслабиться и успокоиться.
Нельзя сдавать кровь сразу после физиотерапевтических процедур, ультразвукового и рентгенологического исследования, массажа и рефлексотерапии.
Перед сдачей крови нужно исключить перепады температур, то есть баню и сауну.
Перед гормональным исследованием крови у женщин репродуктивного возраста следует придерживаться рекомендаций лечащего врача о дне менструального цикла, в который необходимо сдать кровь, так как на результат анализа влияют физиологические факторы фазы менструального цикла.
Перед сдачей крови необходимо успокоиться, чтобы избежать немотивированного выброса в кровь гормонов и увеличение их показателя.
Для сдачи крови на вирусные гепатиты желательно за 2 дня до исследования исключить из рациона цитрусовые, оранжевые фрукты и овощи.
Для правильной оценки и сравнения результатов ваших лабораторных исследований рекомендуется проводить их в одной и той же лаборатории
В разных лабораториях могут применяться разные методы исследования и единицы измерения показателей.
Бак посев можно назвать древним анализом, однако его популярность от этого отнюдь не падает, хотя современная бактериология имеет возможности найти и выделеть не только штаммы, но и отдельной клетки из него, которая называется клоном.
Однако для получения клона необходим специальный прибор – микроманипулятор, который в обычных лабораториях отсутствует, поскольку применяется, в основном, в научно-исследовательских целях (генетические исследования).
Посев менструальной крови на туберкулез
Результат оценивается после трехкратного посева. На посев берутся выделения из влагалища, менструальную кровь, соскоб или смыв эндометрия, содержимое очагов воспаления (например, из язв на шейке матки).
Даже проведение трехкратного посева дает низкий процент высеваемости палочек Коха. В дополнение используют ПЦР полученного биологического материала.
Посев крови на грибковые инфекции
Количественную оценку грибковой инфекции можно дать с помощью посева грибков (культуральный метод).
Для таких целей материал с кожи, ногтей или волос собирают, как и в случае микроскопического исследования, далее:
- Биологический материал переносят в специальную питательную среду.
- Если во взятых образцах были грибки, то через некоторое время вырастают колонии.
- Затем колонии изучаются под микроскопом, что позволяет определить род и вид грибка, а также его концентрацию.
Кроме того, возможно и проведение тестов на чувствительность грибков к определенным противогрибковым препаратам, что позволяет подобрать больному оптимальную схему лечения.
Посев крови на аэробные и анаэробные бактерии
Посев крови необходим для определения возбудителя инфекционного процесса. В норме кровь является стерильной и только при определенной части заболеваний, в нее могут проникать микроорганизмы.
Такой тип инфицирования называется бактериемией.
Наиболее тяжелый вариант бактериемии – сепсис (септицемия, септикопиемия), но данное состояние проявляется яркой клинической картиной и в основном является уделом стационаров (в том числе отделения реанимации).
Не всегда наличие возбудителя в крови приводит к сепсису. Возможна даже физиологическая бактериемия (она кратковременная и может возникать, например, при чистке зубов и неосторожном травмировании десен).
И все же, если микроорганизм попал в кровь, необходимо его выделить, определить и выяснить, к каким антимикробным препаратам он может быть чувствителен.
В этом случае применяется посев на аробные и анаэробные бактерии.
Аэробные бактерии имеют зависимость от кислорода (то есть их размножение без кислорода невозможно или возможно, но очень кратковременно).
Анаэробные бактерии в свою очередь имеют способность размножаться и без присутствия вокруг них источников кислорода.
Другое название для посева на аэробные и анаэробные бактерии является посев крови на стерильность.
Как и в любом другом исследовании, посев может быть ложноотрицательным, это связано со спецификой забора крови при данном исследовании (очень часто, забор крови нужно проводить на высоте лихорадки – повышения температуры тела).
Ложноположительный результат – при несоблюдении правил стерильности лабораторного инструментария, что в современных лабораториях крайне недопустимо и обычно такого не происходит.
В некоторых случаях для подтверждения диагноза необходимо использовать трехкратный посев на стерильность, то есть кровь забирается три раза с небольшим промежутком во времени.
После успешного забора крови для посева на аэробные и анаэробные бактерии, данный материал помещают на питательную среду. В течение определенного времени начинается рост колоний бактерий, присутствующих в кровотоке пациента.
При помощи различных лабораторных тестов исследователь проводит идентификацию бактерии, а также выполняет тест на чувствительность к антибактериальным препаратам, что в дальнейшем поможет лечащему врачу назначить наиболее эффективное лечение болезни.
Бак посев крови на стафилококк
Если возникает подозрение, что в теле развивается стафилококк, в первую очередь, не надо паниковать.
Обнаружение стафилококка клиническом посеве в концентрации 10 в 3 степени при бессимптомном носительстве не угрожает человеку. Вам необходимо обратить внитание на укрепление иммунитета.
Для точного определения, стафилококк ли является возбудителем заболевания, у больного берут на исследование биоматериалы. Это может быть кровь, содержимое гнойничков, отходящая мокрота, а в некоторых ситуациях и спинномозговая жидкость.
Значимые показатели анализа – выявление в сыворотке крови антител к антигенам стафилококка. Для этого используют реакцию торможения гемолиза, реакцию пассивной гемагглютинации. Одновременно проверяется чувствительность бактерии к различным противомикробным препаратам, чтобы в последующем сделать правильный выбор лекарства для борьбы с ним.
В случае если человек относится к группе пациентов с повышенным риском стафилококковой инфекции (из-за перенесенных заболеваний, других причин, вызвавших ослабление иммунной системы), врач может рекомендовать прохождение быстрого теста на коагулазу.
Такое тестирование – надежный способ определения кокков в крови. Если он покажет положительный результат – значит возбудителем стал золотистый стафилококк, если отрицательный – эпидермальный или сапрофитный.
Посев крови на гемокультуру - алгоритм
Итак, материалом для бактериологического посева является кровь в количестве 5 – 10 мл, полученная из локтевой вены.
Участок кожи обрабатывается сначала ватным шариком, смоченным в 70 % - ном этиловом спирте, а затем другим ватным шариком, смоченным в 1 – 2 % - ном растворе йода, до полного высыхания кожи.
Алгоритм здесь может быть такой же, как и при заборе крови вакуумными шприцами с той разницей, что вместо пробирки в переходник вставляется гемокультурный флакон.
В месте венепункции йод вытирают спиртом и заклеивают этот участок пластырем. Пластиковую крышку данного флакона отламывают, обеззараживают внутреннюю поверхность крышки 70 % этиловым спиртом.
При температуре 37°С кровь нужно хранить не более 2–х часов!
Лучше всего произвести посев крови на питательную среду сразу после её забора.
Соотношение крови и питательной среды – 1: 10,осторожно перемешать.
Для получения наиболее достоверного результата проведение анализа должно быть как минимум двоекратным из разных рук с интервалом времени в 30 минут.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
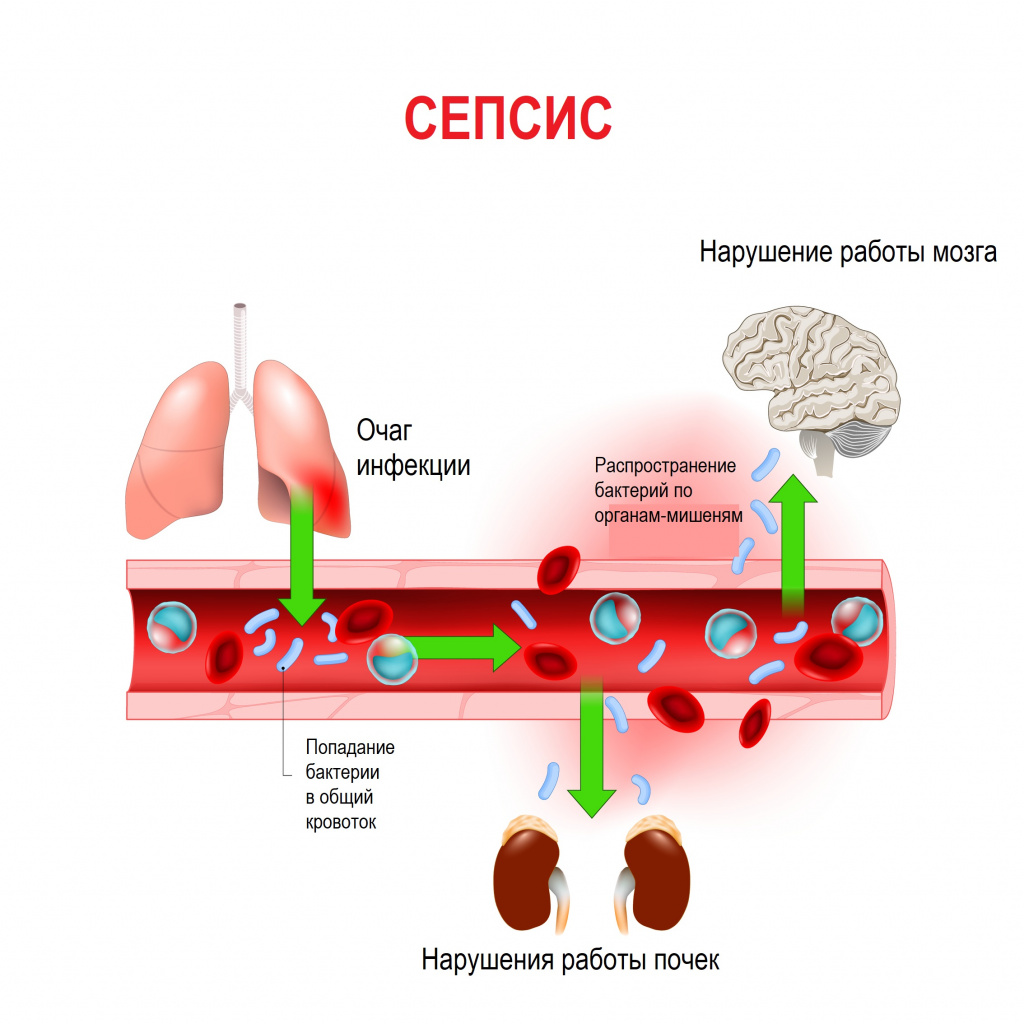
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или 10%.
3. Тяжелый сепсис – сепсис, сочетающийся с полиорганной дисфункцией по двум и более органам, снижением артериального давления № 1700 Маркёры воспаления
Прокальцитонин – высокочувствительный и высокоспецифичный маркер развития бактериальной инфекции и сепсиса.
Читайте также:

