Практическая работа 4 по химии кислород ель получить и собрать кислород
Обновлено: 05.10.2024
FOR-DLE.ru - Всё для твоего DLE ;)
Привет, я Стас ! Я занимаюсь так называемой "вёрсткой" шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и "статейки" для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
ГДЗ Химия 8 класc Габриелян О.С. , Остроумов И.Г., Сладков С.А. 2019 ПРАКТИЧЕСКАЯ РАБОТА 2019 №4 Получение, собирание и распознавание кислорода ОТВЕТЫ

Тушите спиртовку только колпачком (а). Запрещается зажигать одну спиртовку с помощью другой (б). Запрещается передавать спиртовку в зажженном виде (в). Запрещается пробовать вещество на вкус(г). Работу проводить только над столом (д)

Цель работы: научиться использовать лабораторное оборудование и посуду для получения, собирания и доказательства наличия кислорода, соблюдать правила техники безопасности.
Оборудование: аппарат Кирюшкина, лучинка,
Реактивы: перманганат калия KMnO 4 .
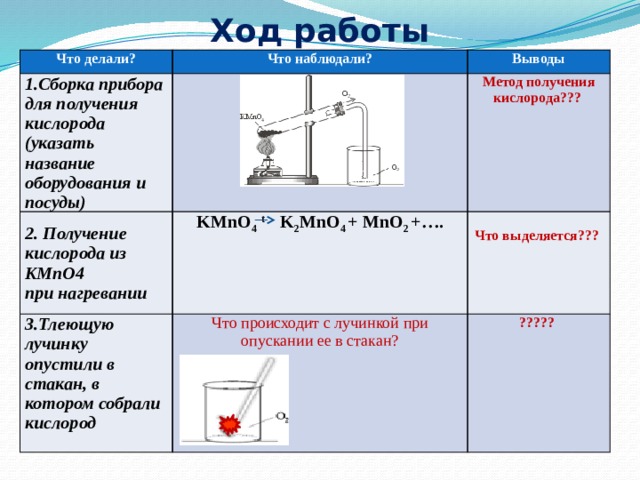
Что наблюдали?
1.Сборка прибора для получения кислорода (указать название оборудования и посуды)
2. Получение кислорода из KMnO4
Метод получения кислорода.
3.Тлеющую лучинку опустили в стакан, в котором собрали кислород
при нагревании
KMnO 4 t K 2 MnO 4 + MnO 2 +….
Цель работы : Получить кислород (методом вытеснения воздуха) и изучить его свойства.
Необходимое оборудование и реактивы
штатив лабораторный с лапкой или пробиркодержатель;
два химических стакана;
пробка с газоотводной трубкой;
ложка для сжигания веществ;
перманганат калия (твердый) KMnO 4 ;
известковая вода - Са(ОН) 2.
Меры предосторожности
Работа со спиртовкой:
Не переносите горящую спиртовку с места на место.
Гасите спиртовку только с помощью колпачка.
При нагревании не забудьте прогреть пробирку. Для этого пробирку, закрепленную в лапке штатива, медленно проведите сквозь пламя от донышка до отверстия и обратно. Эту операцию повторите несколько раз: чтобы стекло равномерно прогрелось. Признаком прогрева стекла можно считать исчезновение запотевания на стенках пробирки.
Дно пробирки должно находиться в верхней части пламени.
Дно пробирки не должно касаться фитиля.
Работа со стеклом:
Помните, что горячее стекло по внешнему виду не отличается от холодного. Не прикасайтесь к горячей пробирке. Закрепляя пробирку в лапке штатива, не закручивайте сильно винт. При нагревании стекло расширяется и пробирка может треснуть
Проверка прибора на герметичность:
Закройте пробирку пробкой с газоотводной трубкой, опустите конец трубки в стакан с водой. Плотно обхватите ладонью пробирку и внимательно следите за появлением пузырьков воздуха.
Загрузите по очереди два следующих видео - опыта и внимательно наблюдайте за экспериментом:
1. Получение кислорода (нажмите "Посмотреть опыт")
Кислород( O 2 ) в лаборатории получают разложением перманганата калия KMnO 4 (марганцовки). Для опыта понадобится пробирка с газоотводной трубкой. В пробирку насыпаем кристаллический перманганат калия. Для сбора кислорода приготовим колбу. При нагревании перманганат калия начинает разлагаться, выделяющийся кислород поступает по газоотводной трубке в колбу. Кислород тяжелее воздуха, поэтому не покидает колбу и постепенно заполняет ее. Тлеющая лучинка вспыхивает в колбе: значит нам удалось собрать кислород.
2KMnO 4 = K 2 MnO 4 + MnO 2 + O 2 ↑
Чистый кислород впервые получили независимо друг от друга шведский химик Шееле (при прокаливании селитры) и английский ученый Пристли (при разложении оксидов ртути и свинца). До их открытия ученые считали, что воздух ‑ однородная субстанция. После открытия Шееле и Пристли Лавуазье создал теорию горения и назвал новый элемент Oxygenium (лат.) – рождающий кислоту, кислород. Кислород - необходим для поддержания жизни. Человек может выдержать без кислорода всего несколько минут.
2. Обнаружение кислорода
Кислород поддерживает горение - это свойство кислорода используется для его обнаружения
Кислород активно взаимодействует со многими веществами. Посмотрим, как реагирует кислород с углем. Для этого раскалим кусочек угля на пламени спиртовки. На воздухе уголь едва тлеет, потому что кислорода в атмосфере около двадцати процентов по объему. В колбе с кислородом уголь раскаляется. Горение углерода становится интенсивным. При сгорании углерода образуется углекислый газ:
С+О 2 = СО 2
Добавим в колбу с газом известковую воду – она мутнеет. Известковая вода обнаруживает углекислый газ. Вспомните, как разжигают гаснущий костер. Дуют на угли или интенсивно обмахивают их для того, чтобы увеличить подачу кислорода в зону горения.
Свидетельство и скидка на обучение каждому участнику
Практическая работа №4
Получение и изучение свойства кислорода
Цель: научиться получать, собирать кислород методом вытеснения воды и методом вытеснения воздуха; изучение физических и химических свойств кислорода; горение угля в кислороде и на воздухе; совершенствовать приемы безопасной работы, проверкой прибора на герметичность.
Оборудование и реактивы: пробирки, газоотводная трубка, стакан химический, ложечка для сжигания, стеклянная пластина, вата, пробка, сухое горючее, спички , п ерманганат калия, сосуд с водой, уголь , сера.
1.Получение и собирание кислорода
а) Получение кислорода методом вытеснения воздуха
1. Вставьте в отверстие выданной вам пробирки с перманганатом калия рыхлый комок ваты и закройте пробирку пробкой с газоотводной трубкой.
2. Проверьте прибор нагерметичность: зажмите пробирку в ладони, опустите конец газоотводной трубки в воду (появление пузырьков воздуха указывает на герметичность прибора).
3. Закрепите собранный прибор в штативе, опустив конец газоотводной трубки в стакан.
4. Нагревайте пробирку (сначала всю, а потом только ту часть, где находится перманганат калия).
5. Собирите кислород методом вытеснения воздуха из стакана . Проверьте, наполнен ли стакан кислородом: поднесите тлеющую лучинку к отверстию стакана, не опуская ее в стакан. Если стакан заполнен кислородом, лучинка вспыхивает и разгорается.
6. Прекратите нагревание, выньте газоотодную трубку из стакана, а стакан быстро закройте стеклянной пластинкой.
б) Получение кислорода методом вытеснения воды
1. Наденьте на конец газоотводной трубки стеклянный наконечник.
2. Наполните пробирку водой и закройте ее пробкой.
3. Опустите пробирку в стакан с водой. Выньте пробку.
4. Опустите трубку с наконечником в стакан с водой (не более 1/2 стакана).
5. Нагрейте пробирку с перманганатом калия до появления выделяющихся пузырьков газа. Находящуюся в стакане пробирку наденьте на конец газоотводной трубки, не вынимая пробирку из воды. Собирите кислород. Докажите его содержание в прбирке (пробирку закройте под водой и выньте из стакана).
2. Горение в кислороде угля и серы
а) Горение угля в кислороде
1. Закрепите уголек на металлической проволоке (препаровальной игле) и внесите в пламя спиртовки.
2. Раскаленный уголек опустите в колбу с кислородом. Что наблюдаете? Дайте объяснение
3. После извлечения несгоревшего угля из колбы, прилейте в нее 5–6 капель известковой воды Са(ОН) 2 . Что наблюдаете? Дайте объяснение.
б) Горение серы в кислороде
1. В железную ложечку положите кусочек серы и подожгите его на пламени.
2. Наблюдайте, как сера горит в воздухе.
3. Затем поместите горящую серу в сосуд с кислородом. (Опыт проводится в вытяжном шкафу).
Читайте также:

